
上海艾力斯医药科技股份有限公司(以下简称“艾力斯”)于近日收到国家药品监督管理局核准签发的《药物临床试验批准通知书》,甲磺酸伏美替尼(以下简称“伏美替尼”)新增适应症的临床研究获得药物临床试验批准。
临床试验批准的相关情况
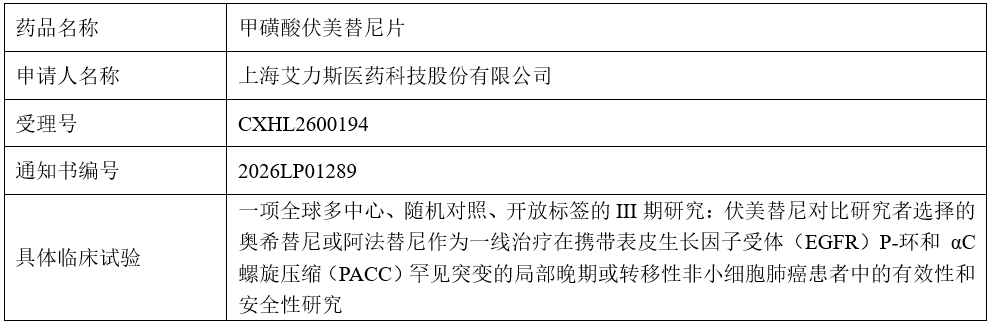
关于伏美替尼
伏美替尼是一种表皮生长因子受体酪氨酸激酶抑制剂(EGFR-TKI),为公司自主研发的1类小分子靶向药,其核心化合物专利创新技术(吡啶胺基嘧啶衍生物、其制备方法及应用)已荣获国家知识产权局、世界知识产权组织联合颁授第二十五届中国专利金奖。
伏美替尼的独特结构不仅增强了与EGFR的结合活性和激酶选择性,改善了代谢特性,抑制非选择性代谢物形成,从而对多种EGFR突变亚型具有较高的靶向选择性,还解决了PACC突变的靶点结合困难,能够通过提升剂量进一步增强对EGFR PACC突变位点的结合力与抑制深度,有效突破治疗瓶颈。EGFR PACC突变约占所有EGFR突变NSCLC患者的12.5%,该突变包含多种亚型,且复合突变多见。根据伏美替尼单药一线治疗EGFR PACC突变晚期NSCLC的一项Ib期全球、随机、多中心、多队列的研究(FURTHER)数据,经BICR评估的240 mg剂量组患者的确认ORR为68.2%, 在包括单一及复合突变中均观察到了肿瘤缓解,证明伏美替尼可实现PACC突变位点全人群覆盖;中位缓解持续时间(DoR)为14.6个月,中位无进展生存期 (mPFS)达到16.0个月,研究中伏美替尼在脑转移患者中也显示出良好的抗肿瘤活性。此外,伏美替尼的安全性良好,未出现新的安全性信号。FURTHER研究充分验证了伏美替尼在EGFR PACC突变NSCLC患者一线治疗中的疗效及安全性。
展望未来,伏美替尼针对EGFR PACC突变患者一线治疗的全球III期关键性研究正在积极开展,以期进一步丰富伏美替尼临床应用循证医学证据,为NSCLC患者群体提供更为全面的应用场景。
关于艾弗沙®
伏美替尼是中国原研、具有自主知识产权的第三代EGFR-TKI,分别于2021年3月、2022年6月获批EGFR突变的局部晚期或转移性NSCLC成人患者的二线、一线治疗适应症,并均已被纳入国家医保目录。2021年6月艾力斯与ArriVent Biopharma, Inc. 达成伏美替尼海外独家授权合作,目前伏美替尼针对EGFR 20号外显子插入突变NSCLC患者一线治疗适应症的包括中国、美国、英国、法国、日本、韩国等多个国家在内的全球多中心III期注册临床研究正在顺利进行中。此外,伏美替尼针对EGFR 20号外显子插入突变NSCLC治疗的适应症获得中、美监管机构的突破性疗法认定;针对NSCLC EGFR敏感突变辅助治疗、PACC 突变NSCLC一线治疗、EGFR 敏感突变NSCLC伴脑转移患者治疗、EGFR非经典突变辅助治疗的注册临床研究也在顺利推进中。
关于艾力斯
上海艾力斯医药科技股份有限公司成立于2004年3月,是一家以全球医药市场需求为导向,专注于肿瘤治疗领域,集新药研发、生产和商业化为一体的创新型制药企业。艾力斯医药以科技关爱生命为发展理念,以开发首创药物和同类最佳药物为首要目标。历经20多年坚持不懈的努力,艾力斯已经成功自主研发,获批多款创新药,具备持续创制具有自主产权的、疗效确切的抗肿瘤新药之综合实力。2020年12月2日,上海艾力斯医药科技股份有限公司正式在上海证券交易所科创板挂牌上市(股票代码:688578)。

